离子运动的三种方式
1. 前言
Mass transfer,标准翻译为“传质”,但我觉得用“物质移动” 更能直观地表达这个概念。
电化学中,“Mass transfer”主要是指电解液中离子的运动。
离子,可被描述为“一种带电荷的物质”。
进一步分拆看:
(1)“物质”,会自发地从高浓度向低浓度移动;
(2)“带电荷”,会受到电势差引起的电场力作用。
(3)此外,诸如搅拌等外力作用,可以造成“带电物质”作为整体发生移动。
因此,离子的移动有三种驱动力:浓度差,电势差,外力。
与之相对应,将产生三种移动方式:扩散,迁移,对流。
2. 三种方式
扩散(diffusion),是浓度差造成的物质移动。
分析物质的扩散要从两个维度来考虑:空间和时间。并由此引出菲克定律(Fick’s laws)。
- 菲克第一定律描述了空间维度的扩散。
-J(x,t)=D\frac{\partial C(x,t)}{\partial x}
其中,D是扩散系数,表征该物质移动能力的强弱。
因为物质移动方向J(x,t)与浓度差方向\frac{\partial C(x,t)}{\partial x} 相反,所以前面加个负号。
- 菲克第二定律描述了时间维度的扩散。
\frac{\partial C(x,t)}{\partial t}=D\left( \frac{\partial^{2}C(x,t)}{\partial x^2} \right)
迁移(migration),是电势差造成的物质移动。
迁移主要作用于远离电极的电解液中,因为这个区域的浓度差较小。可以通过下图近似地描述扩散与迁移主导的区域。
J(x)=-\frac{zF}{RT}DC\frac{\partial \phi (x)}{\partial x}
其中,F,R,T都是常数。
对流(convection),是外力造成的物质移动。
现在假设溶液由于搅拌等外力作用,有了一个力,那么物质移动的量J可定义为浓度
C与速度
\upsilon的乘积:
J(x)=C\upsilon (x)对流有两种基本的模式,一种是一马平川的层流,另一种是有阻隔的湍流。
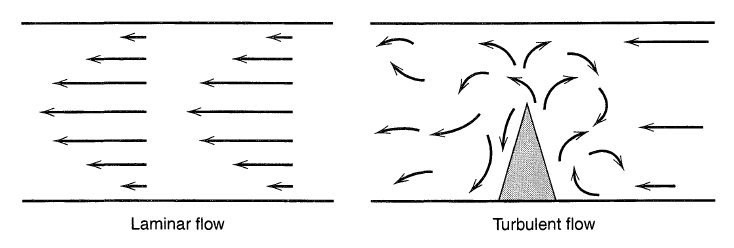
将三者综合起来,且暂不考虑时间维度,可得到电化学中物质移动的通用表达:
J(x)=-D\frac{\partial C(x)}{\partial x} -\frac{zF}{RT}DC\frac{\partial \phi (x)}{\partial x} +C\upsilon (x)
3. 实际分析
将离子的运动分开为三种形式,好处就是可以将一个复杂的体系分割成不同的环节,再进行分析。下面举一个例子。
通过电化学手段可以控制电解液中Cu离子在+1和+2价态之间转变,两种Cu离子浓度都是10^{-3} M , 阴离子为浓度为3\times 10^{-3} M 的Cl^{-} ,其电池示意图如下:

体系中没有搅拌等外力,因此可以忽略对流的作用,可将物质的移动抽象为下图:

以Cathode一侧为例,发生反应Cu^{2+}\rightarrow Cu^{+},造成二者浓度改变,电解液中Cu^{2+}涌向电极,Cu^{+}逃离电极,表现形式为浓度差引起的扩散。Anode一侧发生与之相反的过程。如图中蓝色部分所示。
与此同时,外电路中有电子e通过,因此需要电解液中的离子进行迁移来平衡电势差。即图中所示的红框部分。因为,电解液中离子浓度很低,所以整个体系的电阻很大。
如果我们在这个体系中加入0.1 M的NaClO_{4} 作为额外的电解质,那么迁移与扩散的成分将发生改变,如下图所示。

NaClO_{4} 所提供的离子不发生反应,因此没有电极表面的扩散过程,而仅仅是提供迁移,来平衡电荷。因此,活性成分Cu离子可以更充分地进行反应。即:
反应物专心“迁移”,让跑得快的物质去“扩散"。
类似NaClO_{4} 这种额外的离子,我们称之为支持电解质(supporting electrolyte)。这类电解质除了能降低体系电阻外,还可以提升信号的准确性,调剂电解液整体PH等。
4. 总结
本文介绍了电化学中物质移动的三种形式(扩散,迁移和对流),列出了三者的驱动力和基本公式,并举了一个实例来分拆一个体系中的移动形式。
在物质移动中还有很多有意思的话题,比如扩散系数D是怎么回事,对流的影响是怎样等。以后有机会再写。
参考文献:Bard A J & Faulkner L R, (2003) Electrochemical methods: fundamentals and applications. New York: Wiley.