肺炎支原体感染:基础知识
翻译自:J Gen Fam Med。2017年6月; 18(3):118-125 Mycoplasmapneumoniaeinfection: Basics
摘要
肺炎支原体(Mypoplasma pneumoniae,Mp)是社区获得性肺炎的主要原因之一,并且在没有肺炎的情况下可引起许多肺外表现。在这方面,初级保健医生应该知道如何怀疑,诊断和管理患有Mp感染的患者。本综述概述了Mp感染特别是肺炎的基本临床方面,这将有助于进一步了解该疾病。
关键词:临床特征,概述,肺炎支原体肺炎
1.简介
已知支原体和解脲支原体物种存在于人类中。术语“支原体”(希腊语;“mykes”=真菌和“血浆”=形成)出现于20世纪50年代,并取代了之前的胸膜肺炎样生物(PPLO)术语。肺炎支原体(Mp)长1-2微米,宽0.1-0.2微米,而典型的细菌长1-4微米,宽0.5-1.0微米。Mp的细胞体积小于典型芽孢杆菌的细胞体积的5%。典型的Mp菌落,如图1所示 像琼脂平板上的“煎蛋”,直径很少超过100微米。Mp缺乏细胞壁,这使其对抗菌素(例如通过靶向细胞壁起作用的β-内酰胺类抗菌素)具有内在抗性,因此起引起广泛的临床症状和疾病表现。本文重点介绍了Mp感染的多种临床方面,包括对当前文献的回顾。

图1
琼脂板上肺炎支原体菌落通常有一个独特的“煎鸡蛋”的外观
2. 肺炎支原体的分离历史
1938年,Reimann报告了7名患有异常形式的气管支气管肺炎和严重的全身症状的患者。他认为这种疾病相对于由流感病毒引起的或已知的细菌以及疑似“原发性非典型肺炎”等疾病有着不同临床表现。在20世纪40年代早期,伊顿等人使用棉大鼠,仓鼠,和鸡胚,分离出导致原发性非典型肺炎的主要成因-“伊顿因子” 。1963年,Chanock成功地培养哺乳动物细胞的伊顿因子无细胞培养基,并提出了分类学名称“ 肺炎支原体 ”。更详细的历史可以在Saraya 或Marmion 两篇不同的文章中找到,“肺炎支原体肺炎的历史” 。
3.流行病学
全年都会偶尔发生支原体感染,并且可能发生广泛的社区爆发。日本呼吸学会(JRS)报告,社区获得性肺炎(CAP)患者的Mp肺炎发生率约为5.2%-27.4%。Mp是导致社区获得性肺炎的最常见病原体之一。2005年4月至2008年9月期间,首次进行了一项迄今最大的前瞻性多中心研究日本非典型肺炎,涉及156家日本医疗机构。本研究检查了223名患有性别均分布的Mp肺炎患者,平均年龄为37.9±16.6(平均值±SD)岁。
重要的是,耐大环内酯类抗生素Mp首先于2000年从日本儿童中分离出来,2007年在成人中分离出来,所有患者都具有23S-rRNA突变。在2000年代,在日本和东亚,具有A2063G或A2064G突变的大环内酯抗性Mp的患病率迅速增加,在中国具有显著高的分离率(92%)(图 2)。

图2
各个国家(地区)的大环内酯类耐药肺炎支原体的比例。
4.临床特征
大多数患有Mp感染的患者存在轻微的呼吸道疾病,包括咽炎和气管支气管炎,并且感染通常是自限性的。只有3%-13%的感染者患上肺炎。这种疾病通过飞沫传播,并倾向于在家庭中传播,潜伏期为2-4周。感染的最大风险是5至20岁的年轻人。林等人研究表明,在人们再次感染Mp之前,群体免疫持续约4年(范围:2-10岁)。因此,只有部分免疫可能跟随感染,并且在同一个人中可能发生反复感染。此外,患有低丙种球蛋白血症的人对Mp感染的易感性增加,并且患有镰状细胞病的人可能经历更严重的疾病。
5. Mp肺炎
Mp肺炎的临床表现多种多样(表1),其特征是发烧,不适,头痛和咳嗽的潜伏性发作。持续性咳嗽是Mp感染的临床标志,其严重程度和频率在接下来的1-2天内增加,并且可能变得虚弱。Mp感染具有与呼吸道病毒相似的临床发现,包括但不限于流感病毒和腺病毒。然而,Mp肺炎与那些病毒感染的不同之处在于它具有更缓慢的症状发作,并且腹泻,恶心和呕吐是不常见的。有趣的是,与肺炎球菌肺炎相比,胸膜炎疼痛和颤抖发冷是相对罕见的。
表格1 Mp肺炎临床症状表现的频率
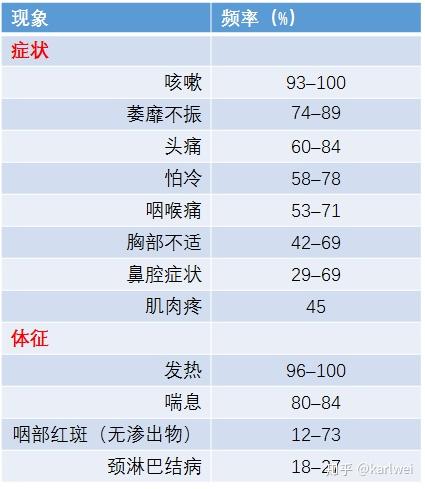
Goto报道,几乎所有Mp肺炎患者根据A-DROP严重程度评分(A,年龄; D,脱水; R,呼吸; O,取向;P,血压等级)分为轻度(85.5%)或中度(14.0%)感染。 由JRS呼吸道感染管理指南委员会制定的A-DROP得分分类感染为轻度(分数:0),中度(评分:1-2),严重(3分),和极重度(得分4-5)。Mp肺炎患者的平均基线体温为37.7±1.0℃。这一趋势与2006年1月至2013年11月期间进行的单中心回顾性研究类似,收集了65 Mp肺炎患者(表 2)。在所有65名患者中,低氧血症仅为12.8%(n = 5),体温为37.9±1.3°C。
表2 65例Mp肺炎患者的特征

在体检中,超过一半的Mp肺炎患者没有听觉噼啪声并且可能有晚期吸气性噼啪声。因此,初级护理医师应该知道这六个因素帮助使用JRS“诊断测试”区分社区获得性肺炎的其他原因引起的Mp肺炎(表 4)。
6.大环内酯类抗性Mp肺炎
2000年后,耐大环内酯类抗生素(MR)Mp在东亚出现并广泛存在。使用大环内酯类药物超过48小时仍然持续发热可能表明存在MR-Mp。在日本,87%的小儿Mp感染是由MR-Mp 引起的,而成人患者的患病率似乎超过30%,主要是由于A2063G突变。如果没有检测23S rRNA基因突变的应用,测定MR-MP是困难的。然而,MR-Mp肺炎患者的发热疾病持续时间明显长于大环内酯类敏感(MS)Mp疾病(1.6±0.8天)患者(4.1±2.3天)。同样,据Suzuki等报道,MR-Mp肺炎患者的发热病持续时间较长,大环内酯给药期间的发热天数(中位数; 8天,3天)比MS-Mp肺炎患者(中位数; 5天,1天)长。另一项研究显示,MR-Mp患者(平均值; 4天,11.4天)开始大环内酯治疗后的发热天数或咳嗽天数显着长于MS-Mp患者(平均1.5天,7天) 。这表明,如果MP-感染者对大环内酯类治疗开始后48小时以上持续发热,我们应该意识到的MR-MP感染的可能性。
危及生命的疾病极为罕见,暴发性Mp肺炎没有明显的危险因素。
7.肺外表现
我们的初步数据显示了Mp肺炎的典型不同症状(图 3)。大约70%的患者出现发烧和咳嗽(通常是干咳)。有趣的是,7%的患者有皮肤病学受累。重要的是,由于Mp感染引起的肺外表现有时在没有Mp肺炎或甚至没有呼吸道症状的情况下发生。如图4所示 ,Mp感染引起各种肺外并发症,如神经,心血管,皮肤病,消化,血液和肌肉骨骼表现,以及其他。神经系统并发症包括脑炎,脑膜脑炎,无菌性脑膜炎,脊髓炎,多发性神经炎和精神病。中枢神经系统表现在每1000例不到1例中发生,并且最常见于住院患者。还报道了格林 - 巴利综合征和周围神经病变。CNS受累的发病机制尚不清楚,但是直接侵入生物体,产生毒素和自身免疫(自身抗体的产生)是可能的机制。心血管表现包括心包炎,心内膜炎和心肌炎。症状和体征是心律失常,充血性衰竭,胸痛和心电图异常,特别是传导缺陷。在患有心包炎的患者中,Mp经常从心包液和/或组织中分离。关于皮肤病,Stevens-Johnson综合征和多形性红斑与Mp感染有关。还报道了肝脏受累,其特征在于发烧后7-10天肝功能障碍。然而,我们的初步数据包括患有Mp肺炎的儿童(n = 72)和成人(n = 54),他们很少表现出血清丙氨酸氨基转移酶的紊乱。另一方面,儿童天冬氨酸氨基转移酶升高的频率显着高于成人,这可能反映了肌肉骨骼受累导致的轻度横纹肌溶解症。在血液学表现中,自身免疫性溶血性贫血是最常见的间接肺外受累。其他疾病,如噬血细胞综合征,被认为是细胞因子 - 风暴疾病,并且高凝状态可以表现为弥散性血管内凝血。关节炎和横纹肌溶解等肌肉骨骼疾病很少见,但可以看出。其他疾病(粘膜炎,中耳炎和肾小球肾炎)也偶尔被认可。

图3
在Kyorin大学治疗的54例肺炎支原体肺炎患者的症状

图4
有或没有肺外受累的肺炎支原体感染的分类。DIC,弥散性血管内凝血
8. Mp肺炎的发病机制
Mp呼吸道疾病的严重程度似乎与宿主免疫应答对感染的反应程度有关。我们的“小鼠模型”证实了这种情况对于各种条件致敏的Mp肺炎。肺炎支原体附着于支气管上皮细胞,通过表面粘附分子,所述蛋白质P1介导的。
已经认识到Mp的几种毒力机制,包括(i)脂蛋白/脂肽,(ii)社区获得性呼吸窘迫综合征(CARDS)毒素,和(iii)其他因素(溶血素,过氧化氢和超氧化物自由基)(图 5))。Mp具有具有有效炎性的脂蛋白/脂肽,其通过Toll样受体TLR1,TLR2和TLR6被宿主免疫系统(即支气管上皮细胞和肺泡巨噬细胞)识别。最近,Shimizu等人报道TLR4和自噬在诱导TLR2非依赖性途径中起重要作用。最近,Kannan等人认可了CARDS毒素,这与Mp疾病的病理生理学有关。该毒素与气道上皮细胞上的人表面活性蛋白A和膜联蛋白A2结合并被内化,导致一系列致病事件。其他因素因氧化应激的有害影响而众所周知。
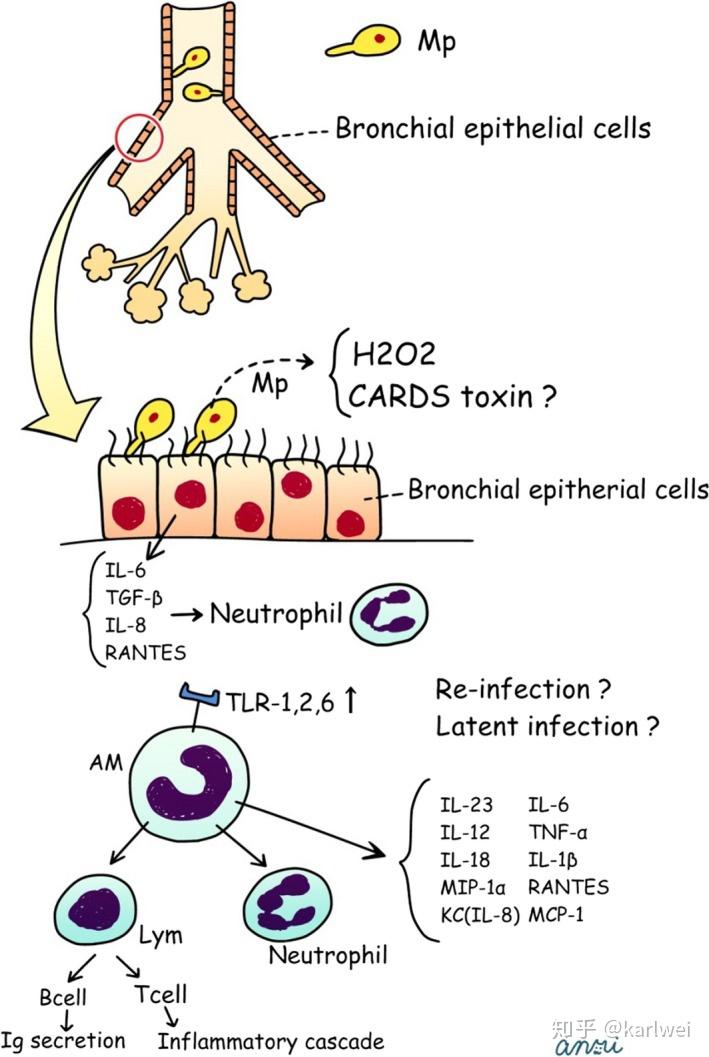
图5
用于产生人肺炎支原体肺炎过程的假定模式。CARDS,社区获得性呼吸窘迫综合征; 肿瘤坏死因子,肿瘤坏死因子; RANTES,受激活调节,正常T细胞表达和分泌; MCP-1,单核细胞趋化蛋白-1。
9. 肺炎支原体与支气管哮喘的关系
一些报道称Mp感染可能与儿童而不是成人哮喘急性发作相关。矢野等人报道,上呼吸道支原体呼吸道感染涉及通过MP-特异性IgE介导的过敏性气道炎症的复杂的相互作用,导致初始喘憋症状。卡夫特等人表明甚至在慢性,稳定的成人哮喘患者的气道中也可以检测到Mp。因此,潜伏的Mp感染和无症状的携带状态可能在慢性哮喘或哮喘恶化的发病机理中起作用。然而,我们的数据表明,哮喘急性发作与Mp感染无关,而是与多达约50%的住院哮喘患者的病毒感染(即人鼻病毒,人间质肺病毒和呼吸道合胞病毒)有关。
10.人类病理学和支气管肺泡灌洗液的发现
几乎没有报道Mp肺炎的病理结果。然而,一些报道已经讨论了基于不同组织的诊断技术,例如经支气管肺活检,胸腔镜手术,开放肺活检,和尸检。根据之前的报道,Mp肺炎的特征性病理特征是在肺血管周围区域(PBVAs)中有明显的浆细胞丰富的淋巴细胞浸润,在肺泡腔中积聚了巨噬细胞,中性粒细胞和淋巴细胞。
有趣的是,直到最近仍然关于Mp肺炎的支气管肺泡灌洗液分析的报道仍然很稀少。有几个研究表明,中性粒细胞和淋巴细胞增加比其他类型的细胞更多。在支气管肺泡灌洗液(BALF)的CD4到CD8升高比率在不同的采样周期里介于2.1至3.5±2.1之间 。
11.诊断方法
尽管冷凝集素的存在不是特异性的,但是1:64或更高的滴度提示Mp感染。培养是诊断Mp感染的金标准方法;,但是确定结果需要1-2周,因此很少进行。血清学方法如颗粒凝集(PA),补体结合(CF),和快速诊断诸如ImmunoCard ®(IC)(免疫球蛋白支原体M [IgM型])是市售的。环介导等温扩增(LAMP)方法和快速抗原检测(Ribotest;旭化成制药公司,日本)使用咽拭子也可商购。
如果CF滴度高于1:64或PA滴度高于1:320,则可以诊断为Mp感染。在以前的报告中,IC支原体检测的结果与PA检测的结果不一致,特别是在成人中,这需要在成人诊断中提高四倍的滴度(表 3)。
表3 Mp肺炎的诊断方法

虽然少数实验室可以使用基于PCR的诊断,但Mp感染的敏感性和特异性分别为40.7%-66.7%和88.8%-98.5%,血清学诊断作为参考标准。LAMP法是一种新型的核酸扩增方法,可通过咽拭子快速检测Mp,于2010年在日本上市,其检测Mp的敏感性和特异性与PCR相同。血清学测试的结果被认为是标准的,在灵敏度,特异性,和LAMP检测的阳性和阴性预测值分别为94.8%,91.9%,91.1%,和95.2%之间。有人通过LAMP测定法测量的咽部携带的中位持续时间为9.5天。当将LAMP测定与经验证的实时PCR测试进行比较时,LAMP测定的灵敏度在提取的核酸上测试为88.5%,在未提取的临床样本上评估为82.1%。在这方面,LAMP检测可以快速(在几个小时内)低成本检测Mp感染。最佳样本位点在病原体或年龄方面有所不同。在通过成人患者的核酸扩增方法检测Mp时,痰可能优于鼻咽拭子或口咽拭子。
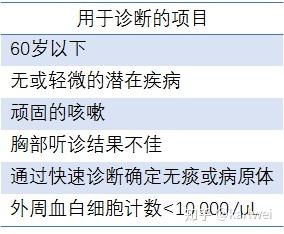
Ribotest Mp(Asahi Kasei Pharma Corp)是一种快速抗原试剂盒,用于使用免疫色谱法检测Mp核糖体蛋白L7 / L12,于2013年在日本上市。另一项研究显示该试验的Mp阈值为1.1×10 4 cfu / mL。然而,随着PCR相比Ribotest的诊断灵敏度不高,大约60%。从这个角度来看,Mp肺炎的诊断应该基于JRS 提出的以下六个因素:(i)<60岁; (ii)缺少或仅有轻微的潜在疾病; (iii)顽固的咳嗽; (iv)胸部听诊的异常发现; (v)通过快速诊断测试没有痰或存在可识别的病原体; (vi)外周血白细胞计数<10000 /μL(表 4)。如果存在四种或更多种提出的因子,则可以容易地将Mp肺炎与其他病原体区分开来,具有高灵敏度(88.7%)和中等特异性(77.5%)。
表4 Mp肺炎患者的特征
12.放射学特征
在我们未发表的数据中,患有Mp肺炎的儿童和成人的胸部X射线的一个突出特征是实变,接着是磨玻璃样混浊,主要见于中下肺野。
关于Mp肺炎的胸部计算机断层扫描,到目前为止仅报告了几个小病例系列。放射学发现多种多样; 然而,整合(见图 6A),磨碎的玻璃影(图 6B),和支气管血管束增厚(图 6C)与支气管血管周围(图 6B,C)或小叶中心结节(图 6d)是Mp肺炎中的突出特征。与肺炎链球菌肺炎进行鉴别对比,小叶中心结节的存在提示存在Mp肺炎。
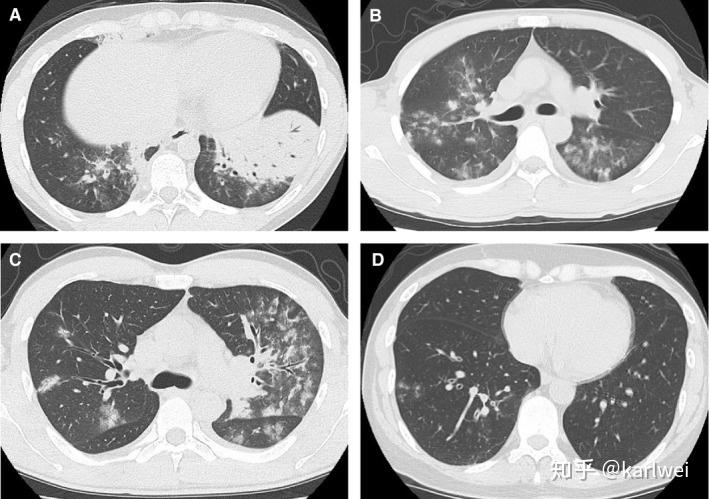
图6
胸部计算机断层扫描显示左下肺叶大量实变,空气支气管造影(A),支气管血管周围区域(B,C)的GGO伴支气管血管束增厚(C)。(D)显示具有支气管增厚的小叶中心结节。GGO,磨砂玻璃不透明
13.治疗
大环内酯类对中性粒细胞功能和炎症级联中涉及的细胞因子的产生具有直接影响。它们的口服生物利用度为50%,组织浓度高达上皮衬里液,肺泡巨噬细胞和中性粒细胞中血清浓度的300倍。关于MP感染,14-或15-元环大环内酯通常被认为是一线剂,其用于抗炎,免疫调节作用是广泛认可的。
尽管JRS指南没有涉及Mp肺炎的治疗方案(表5),但日本支原学会建议了门诊病人的一线疗法(口服克拉霉素[CAM] 200 mg bid 7-10天或阿奇霉素[AZM] 2 g一次或AZM 500 mg / d三天或红霉素[EM] 800 mg-1200 mg / d 7-10天)和二线口服治疗(minomycin [美浓霉素MINO] 200 mg / d或氟喹诺酮治疗7-10天)。在住院患者中,该学会建议静脉注射美浓霉素MINO 200 mg / d或EM 600 mg-1500 mg / d治疗7-10天,或阿奇霉素AZM 500 mg仅作为一线治疗,静脉注射氟喹诺酮类药物作为二线治疗。作为辅助疗法的全身性类固醇治疗可以改善严重Mp肺炎的结果,但效果还是有争议的。
表5 不同指南推荐治疗Mp肺炎的治疗药物

JRS,日本呼吸学会; IDSA,美国传染病学会; 美国胸科学会ATS; BTS,英国胸科学会。
无论是门诊还是住院病人,如果大环内酯类药物开始后48-72小时发热持续,建议口服或静脉注射美浓霉素MINO 200 mg / d作为MR-Mp治疗。美国传染病学会/美国胸科协会或英国胸科学会指南推荐的Mp肺炎治疗方法如表5所示 。这些治疗旨在用于广谱初始覆盖,并且不打算在初始治疗时区分非典型病原体与其他社区获得性肺炎病原体。
MP肺炎可以表现出不同的临床效果,对于初级保健医生来说,诊断有时可能具有挑战性。然而,对Mp感染的各种临床表现的理解和认识可以导致更准确的诊断和有效的治疗。

